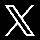Azufre
Azufre. Es un elemento químico de número atómico 16 y símbolo S (del latín sulphur). Es un no metal abundante con un olor característico. El azufre se encuentra en forma nativa en regiones volcánicas y en sus formas reducidas formando sulfuros y sulfosales o bien en sus formas oxidadas como sulfatos. Es un elemento químico esencial para todos los organismos y necesario para muchos aminoácidos y, por consiguiente, también para las proteínas.
Sumario
Características principales
Este no metal tiene un color amarillento, amarronado o anaranjado, es blando, frágil, ligero, desprende un olor característico a huevo podrido al combinarse con hidrógeno y arde con llama de color azul, desprendiendo dióxido de azufre. Es insoluble en agua pero se disuelve en disulfuro de carbono. Es multivalente, y son comunes los estados de oxidación -2, +2, +4 y +6. En todos los estados (sólido, líquido y gaseoso) presenta formas alotrópicas cuyas relaciones no son completamente conocidas.
Las estructuras cristalinas más comunes son el octaedro ortorrómbico (azufre α) y el prisma monoclínico (azufre β), siendo la temperatura de transición de una a otra de 96 °C; en ambos casos el azufre se encuentra formando moléculas de S8 con forma de anillo, y es la diferente disposición de estas moléculas la que provoca las distintas estructuras cristalinas.
A temperatura ambiente, la transformación del azufre monoclínico en ortorrómbico, es más estable y muy lenta. Al fundir el azufre, se obtiene un líquido que fluye con facilidad formado por moléculas de S8. Sin embargo, si se calienta, el color se torna marrón algo rojizo, y se incrementa la viscosidad.
Este comportamiento se debe a la ruptura de los anillos y la formación de largas cadenas de átomos de azufre, que pueden alcanzar varios miles de átomos de longitud, que se enredan entre sí disminuyendo la fluidez del líquido; el máximo de la viscosidad se alcanza en torno a los 200 °C.
Enfriando rápidamente este líquido viscoso se obtiene una masa elástica, de consistencia similar a la de la goma, denominada «azufre plástico» (azufre γ) formada por cadenas que no han tenido tiempo de reordenarse para formar moléculas de S8; transcurrido cierto tiempo la masa pierde su elasticidad cristalizando en el sistema rómbico. Estudios realizados con rayos X muestran que esta forma amorfa puede estar constituida por moléculas de S8 con estructura de hélice espiral.
En estado vapor también forma moléculas de S8, pero a 780 °C ya se alcanza el equilibrio con moléculas diatómicas y por encima de aproximadamente 1800 °C la disociación es completa y se encuentran átomos de azufre. Además de en trozos, barras o polvo grueso, existe en el mercado una presentación en forma de polvo muy fino, llamada "Flor de azufre", que puede obtenerse por precipitación en medio líquido o por sublimación de su vapor sobre una placa metálica fría.
Aplicaciones
El azufre se usa en multitud de procesos industriales como la producción de ácido sulfúrico para baterías y el vulcanizado del caucho y principalmente como fertilizante, fabricación de pólvora, laxantes, cerillas e insecticidas; también como fungicida y en la manufactura de fosfatos fertilizantes.
Los sulfitos se usan para blanquear el papel y en cerillas. El tiosulfato de sodio o amonio se emplea en la industria fotográfica como «fijador» ya que disuelve el bromuro de plata; y el sulfato de magnesio (sal de Epsom) tiene usos diversos como laxante, exfoliante, o suplemento nutritivo para plantas.
Abundancia y obtención
El azufre es un elemento muy abundante en la corteza terrestre, se encuentra en grandes cantidades combinado en forma de sulfuros (pirita, galena) y de sulfatos (aljez). En forma nativa se encuentra en las cercanías de aguas termales, zonas volcánicas y en minas de cinabrio, galena, esfalerita y estibina, y en Luisiana (Estados Unidos, primer productor mundial) se extrae mediante el proceso Frasch consistente en inyectar vapor de agua sobrecalentado para fundir el azufre que posteriormente es bombeado al exterior utilizando aire comprimido. En Cuba hay yacimientos de pirita, que es el azufre en forma de sulfuro, en la provincia de Pinar del Río y en Las Villas.
También se obtiene separándolo de gas natural, si bien su obtención anteriormente era a partir de depósitos de azufre puro impregnado en cenizas volcánicas (Italia, y más recientemente Argentina). Un compuesto natural del azufre es el yeso (CaSO4.2H2O), de gran importancia económica.
También está presente, en pequeñas cantidades, en combustibles fósiles (carbón y petróleo) cuya combustión produce dióxido de azufre que combinado con agua produce la lluvia ácida; para evitarlo las legislaciones de los países industrializados exigen la reducción del contenido de azufre de los combustibles, constituyendo este azufre, posteriormente refinado, un porcentaje importante del total producido en el mundo.
También se extrae del gas natural que contiene sulfuro de hidrógeno que una vez separado se quema para obtener azufre: 2 H2S + O2 → 2 S + 2 H2O El color distintivo de Ío, la luna volcánica de Júpiter, se debe a la presencia de diferentes formas de azufre en estado líquido, sólido y gaseoso.
El azufre se encuentra, además, en varios tipos de meteoritos, y se cree que la mancha oscura que puede observarse cerca del cráter lunar Aristarco puede ser un depósito de azufre. El azufre también se encuentra formando parte de muchas sustancias orgánicas de origen animal y vegetal (huevos, aceites de ajos, mostaza, proteínas, etc.)
Compuestos
Muchos de los olores desagradables de la materia orgánica se deben a compuestos de la materia que contienen azufre como el sulfuro de hidrógeno. Disuelto en agua es ácido (pKa1 = 7,00, pKa2 = 12,92) y reacciona con los metales.
Los sulfuros metálicos se encuentran en la naturaleza, sobre todo el de hierro (pirita) que puede presentar resistencia negativa y la galena, sulfuro de plomo que es un semiconductor natural que fue usado como rectificador.
El nitruro de azufre polímero (SN)x, sintetizado en 1975 por Alan G. MacDiarmid y Alan J. Heeger, presenta propiedades metálicas, a pesar de estar constituido por no metales, e inusuales propiedades eléctricas y ópticas.
Este trabajo sirvió de base para el posterior desarrollo, con Hideki Shirakawa, de plásticos conductores y semiconductores que motivó la concesión del Nobel de Química, en 2000, a los tres investigadores. Los óxidos más importantes son el dióxido de azufre, SO2 (formado por la combustión del azufre) que en agua forma una solución de ácido sulfuroso, y el trióxido de azufre, SO3, que en solución forma el ácido sulfúrico; siendo los sulfitos y sulfatos las sales respectivas.
Isotopía
Se conocen 18 isótopos del azufre, cuatro de los cuales son estables: S-32 (95,02%), S-33 (0,75%), S-34 (4,21%) y S-36 (0,02%). Aparte del S-35, formado al incidir la radiación cósmica sobre el argón-40 atmosférico y que tiene un periodo de semidesintegración de 87 días, los demás isótopos radiactivos son de vida corta.
Precauciones
El disulfuro de carbono, el sulfuro de hidrógeno (sulfhídrico), y el dióxido de azufre deben manejarse con precaución. El sulfhídrico y algunos de sus derivados, los mercaptanos, son bastante tóxicos (más que cianuro). Aunque muy maloliente incluso en concentraciones bajas, cuando la concentración se incrementa el sentido del olfato rápidamente se satura o se narcotiza desapareciendo el olor por lo que a las víctimas potenciales de la exposición les puede pasar desapercibida su presencia en el aire hasta que se manifiestan sus efectos, posiblemente mortales.
El dióxido de azufre reacciona con el agua atmosférica para producir la lluvia ácida. Irrita las mucosidades y los ojos y provoca tos al ser inhalado. Los vapores del ácido sulfúrico pueden provocar hemorragias en los pulmones, llenándolos de sangre con la consiguientemente asfixia.
Efectos del Azufre sobre la salud
El azufre se puede encontrar frecuentemente en la naturaleza en forma de sulfuros. Durante diversos procesos se añaden al medio ambiente enlaces de azufre dañinos para los animales y los hombres.
Estos enlaces de azufre dañinos también se forman en la naturaleza durante diversas reacciones, sobre todo cuando se han añadido sustancias que no están presentes de forma natural. Los compuestos del azufre presentan un olor desagradable y a menudo son altamente tóxicos. En general las sustancias sulfurosas pueden tener los siguientes efectos en la salud humana:
- Efectos neurológicos y cambios comportamentales
- Alteración de la circulación sanguínea
- Daños cardiacos
- Efectos en los ojos y en la vista
- Fallos reproductores
- Daños al sistema inmunitario
- Desórdenes estomacales y gastrointestinales
- Daños en las funciones del hígado y los riñones
- Defectos en la audición
- Alteraciones del metabolismo hormonal
- Efectos dermatológicos
- Asfixia y embolia pulmonar
Efectos ambientales del Azufre
El azufre puede encontrarse en el aire en varias formas diferentes. Puede provocar irritaciones en los ojos y garganta de los animales, cuando la toma tiene lugar a través de la inhalación del azufre en su fase gaseosa. El azufre se aplica extensivamente en las industrias y es emitido al aire, debido a las limitadas posibilidades de destrucción de los enlaces de azufre que se aplican.
Los efectos dañinos del azufre en los animales son principalmente daños cerebrales, a través de un malfuncionamiento del hipotálamo, y perjudicar el sistema nervioso. Pruebas de laboratorio con animales de prueba han indicado que el azufre puede causar graves daños vasculares en las venas del cerebro, corazón y riñones.
Estos tests también han indicado que ciertas formas del azufre pueden causar daños fetales y efectos congénitos. Las madres pueden incluso transmitirles envenenamiento por azufre a sus hijos a través de la leche materna. Por último, el azufre puede dañar los sistemas enzimáticos internos de los animales.